
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:35.
- Última modificación 2025-01-22 16:57.
¿En qué se diferencia el agua por debajo de su punto de fusión y por encima? ¿eso? Debajo se mantienen juntos y rebotan entre sí. Encima las moléculas se acercan aún más que debajo . los hirviendo /condensación punto de agua es 373K.
Por lo tanto, ¿por qué los puntos de fusión y congelación son los mismos?
Congelación y derritiendo son solo términos diferentes que se usan para describir la transición entre los estados sólido y líquido de un material. Congelación Por lo general, significa que se está eliminando energía de un material (el líquido se está convirtiendo en sólido) y derritiendo generalmente significa que se está agregando energía a un material (el sólido se está transformando en líquido).
Uno también puede preguntarse, ¿el agua reduce el punto de fusión? Derritiendo absorbe calor ("calor latente") porque el líquido tiene más energía que el sólido. Que enfría el hielo y lo salado agua a menos de 0 ° C. Entonces si, es baja la temperatura real.
De manera similar, puede preguntar, ¿cómo sabrá si el punto de fusión de un compuesto está por encima o por debajo de la temperatura ambiente?
Si los punto de fusión normal de una sustancia es por debajo de la temperatura ambiente , los sustancia es un líquido en temperatura ambiente . Benceno se derrite a 6 ° C y hierve a 80 ° C; es un líquido en temperatura ambiente . Si ambos punto de fusión normal y el punto de ebullición normal están por encima de la temperatura ambiente , los sustancia es un sólido.
¿Qué sustancia tiene un punto de fusión más alto que el agua?
El cloruro de sodio se funde a 801 ° C. Hielo (sólido H 2 O) es un compuesto molecular cuyas moléculas se mantienen unidas por hidrógeno cautiverio. Aunque hidrógeno Los enlaces son la más fuerte de las fuerzas intermoleculares, la fuerza de hidrógeno enlaces es mucho menor que el de los enlaces iónicos.
Punto de fusion.
| Material | Punto de fusión (° C) |
|---|---|
| planchar | 1538 |
Recomendado:
¿El agua tiene un punto de fusión bajo?

El agua en realidad no tiene un punto de fusión bajo en comparación con otros compuestos covalentes. La mayoría de los compuestos covalentes de masa molar baja son gaseosos a temperatura ambiente, mientras que el agua es líquida. Los enlaces covalentes son lo suficientemente fuertes, pero están limitados a moléculas individuales, no a la parte completa del compuesto
¿Por qué el punto de fusión del diamante es más alto que el del grafito?

En el diamante de valencia, los electrones están completamente unidos de forma covalente. Pero en el grafito solo tres están unidos covalentemente mientras que un electrón se mueve libremente, por lo que parece que el punto de fusión del diamante debería ser más alto que el del grafito porque en el diamante debemos romper cuatro enlaces covalentes mientras que en el grafito solo tres enlaces
¿Por qué el agua tiene un alto punto de fusión?
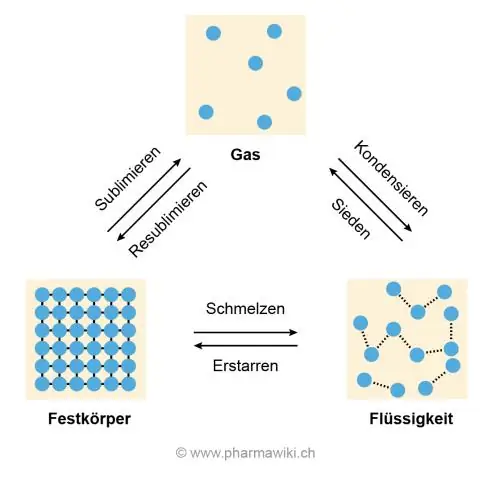
La razón de las altas temperaturas de fusión y ebullición es el enlace de hidrógeno entre las moléculas de agua que hace que se peguen y resistan ser separados, que es lo que sucede cuando el hielo se derrite y el agua hierve para convertirse en gas
¿Por qué el aluminio tiene un punto de fusión más alto que el sodio?

A lo largo del período, la valencia aumenta (desde la valencia 1 en sodio hasta la valencia 3 en aluminio), por lo que los átomos de metal pueden deslocalizar más electrones para formar cationes cargados positivamente y un mar más grande de electrones deslocalizados. Por lo tanto, el enlace metálico se vuelve más fuerte y el punto de fusión aumenta del sodio al aluminio
¿Por qué el agua tiene un punto de ebullición y un punto de fusión altos?

La razón de las altas temperaturas de fusión y ebullición es el enlace de hidrógeno entre las moléculas de agua que hace que se peguen y resistan ser separados, que es lo que sucede cuando el hielo se derrite y el agua hierve para convertirse en gas
