
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:35.
- Última modificación 2025-01-22 16:57.
Cuando Δ GRAMO < 0 Delta ext GRAMO < 0 Δ GRAMO < 0 delta, texto de inicio, GRAMO , end text, es menor que, 0 , el proceso es exergónico y procederá espontáneamente en la dirección de avance para formar más productos. Eso significa que las concentraciones de reactivos y productos permanecerán constantes en equilibrio.
También la pregunta es, ¿qué sucede cuando Delta G es cero?
Las reacciones desfavorables han Delta G valores que son positivos (también llamados reacciones endergónicas). Cuando el Delta G porque una reacción es cero , se dice que una reacción está en equilibrio. Equilibrio NO significa concentraciones iguales. Si el Delta G es cero , no hay cambio neto en A y B, ya que el sistema está en equilibrio.
De manera similar, ¿qué sucede si la energía libre de Gibbs es negativa? Energía libre de Gibbs es una cantidad derivada que combina las dos grandes fuerzas impulsoras en los procesos químicos y físicos, a saber, el cambio de entalpía y el cambio de entropía. Si los la energía libre es negativa , estamos viendo cambios en la entalpía y la entropía que favorecen el proceso y ocurre espontáneamente.
Asimismo, ¿es una reacción espontánea cuando Delta G es 0?
Delta G es igual a 0 . Cuando delta G es positivo, el reacción no es espontáneo . Cuando es negativo, es espontáneo.
¿Por qué la energía libre de Gibbs es 0 en equilibrio?
Energía libre de Gibbs es una medida de cuánto "potencial" le queda a una reacción para hacer un "algo" neto. Entonces si el energía gratis es cero, entonces la reacción está en equilibrio , no se puede hacer más trabajo. Puede ser más fácil ver esto usando una forma alternativa de la Energía libre de Gibbs , como ΔG = −TΔS.
Recomendado:
¿Qué le pasa al azúcar cuando lo agregamos al aceite?

El azúcar se disuelve fácilmente en agua y el aceite no. El agua tiene una baja solubilidad cuando se trata de aceite. Dado que el aceite no es soluble en agua, nunca se disolverá realmente
¿Por qué el EMF es cero cuando la bobina pasa por el centro exacto del imán?
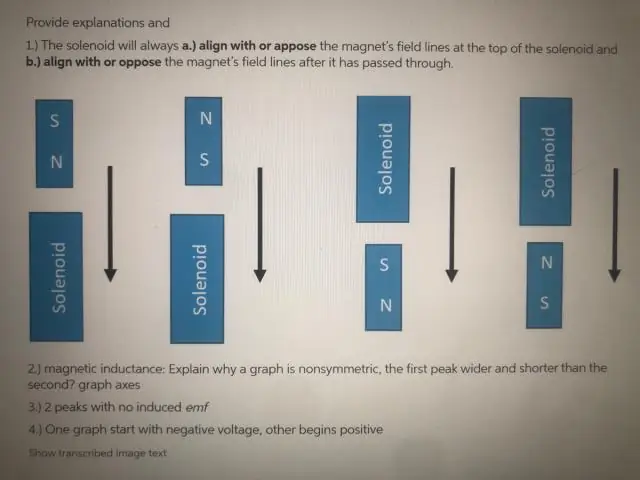
La fem es solo cero por un instante cuando el imán pasa por el centro exacto de la bobina. Esto se debe a que el efecto del polo N en un extremo del imán en ese extremo de la bobina se cancela exactamente por el efecto del polo S del imán en el otro extremo de la bobina
¿Qué pasa cuando se calienta la sal?

En pocas palabras, si calienta una sustancia (como la sal) mucho más allá de la temperatura del punto de ebullición del agua, el efecto Leidenfrost puede ocurrir y resultar en lo que se llama una explosión de vapor. Una vez que la sal se vierte en el agua, el vapor alrededor de la sal se sobrecalienta, provocando un aumento de presión
¿Qué pasa cuando restas vectores?

Physics I For Dummies, 2ª edición Para restar dos vectores, coloque sus pies (o colas, las partes no puntiagudas) juntas; luego dibuja el vector resultante, que es la diferencia de los dos vectores, desde la cabeza del vector que estás restando hasta la cabeza del vector del que lo estás restando
¿Cuándo debería utilizar la correlación y cuándo debería utilizar la regresión lineal simple?
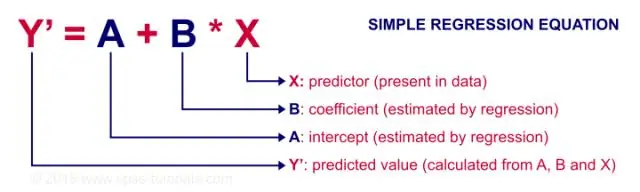
La regresión se usa principalmente para construir modelos / ecuaciones para predecir una respuesta clave, Y, a partir de un conjunto de variables predictoras (X). La correlación se utiliza principalmente para resumir de forma rápida y concisa la dirección y la fuerza de las relaciones entre un conjunto de 2 o más variables numéricas
