- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:35.
- Última modificación 2025-01-22 16:57.
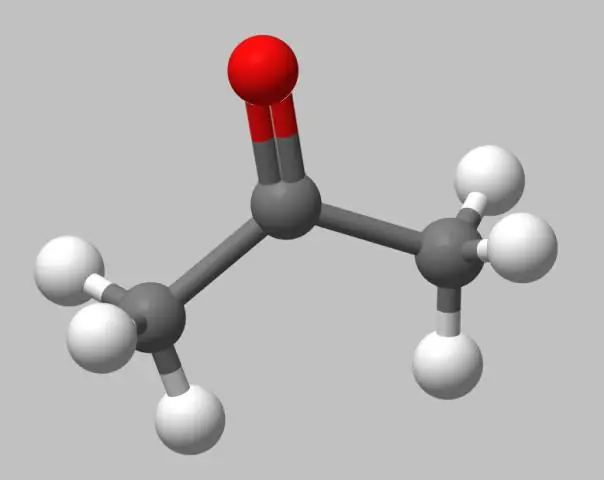
Modelos de bola y palo . Modelos de bola y palo no son tan realistas como llenar el espacio modelos , porque los átomos se representan como esferas de radios más pequeños que sus radios de van der Waals. Sin embargo, el arreglo de enlace es más fácil de ver porque los enlaces se representan explícitamente como palos.
Posteriormente, también cabe preguntarse, ¿qué representa el modelo de pelota y palo?
En química, el modelo de pelota y palo es un molecular modelo de una sustancia química que debe mostrar tanto la posición tridimensional de los átomos como los enlaces entre ellos. Los átomos son típicamente representado por esferas, conectadas por varillas que representar los lazos.
Además, ¿en qué se diferencia un modelo de llenado de espacio de un modelo de bola y palo? Modelos de pelota y palo son tridimensionales modelos donde los átomos están representados por esferas de diferente los colores y los enlaces están representados por palos entre las esferas. Modelos de relleno de espacio son similares a modelos de pelota y palo en que son tridimensionales modelos que representan los átomos como esferas coloreadas.
Aquí, ¿por qué el modelo de bola y palo no es exacto?
los modelo de pelota y palo es no a cierto representación de la estructura del sulfuro de potasio. 3.3) El azufre también puede formar enlaces covalentes. 3.6) Los compuestos iónicos como el sulfuro de potasio tienen altos puntos de ebullición y conducen la electricidad cuando se disuelven en agua.
¿El agua es polar o no polar?
Agua (H2O) es polar debido a la forma doblada de la molécula. La forma significa que la mayor parte de la carga negativa del oxígeno en el lado de la molécula y la carga positiva de los átomos de hidrógeno está en el otro lado de la molécula. Esto es un ejemplo de polar enlace químico covalente.
Recomendado:
¿Cómo se traduce una imagen en matemáticas?
VIDEO En este sentido, ¿cómo se traduce una imagen en matemáticas? en un traducción , cada punto del objeto debe moverse en la misma dirección y por la misma distancia. Cuando realiza una traducción , el objeto inicial se llama pre imagen , y el objeto después del traducción se llama el imagen .
¿Qué es la sal de una imagen en un espejo plano?

SAL. Es la imagen delante o detrás del espejo. ¿Está la imagen más cerca o más lejos del espejo que el objeto?
¿Por qué el modelo de Rutherford se llama modelo nuclear?

El modelo del átomo de Rutherford se llama átomo nuclear porque fue el primer modelo atómico en presentar un núcleo en su núcleo
¿Por qué Hardy Weinberg no es realista?

Cuando una población está en equilibrio Hardy-Weinberg para un gen, no está evolucionando y las frecuencias alélicas permanecerán iguales a lo largo de las generaciones. Son: mutación, apareamiento no aleatorio, flujo de genes, tamaño de población finito (deriva genética) y selección natural
¿Por qué podría llamarse al modelo de Bohr un modelo planetario del átomo?

La razón por la que se llama 'modelo planetario' es que los electrones se mueven alrededor del núcleo de manera muy similar a como los planetas se mueven alrededor del sol (excepto que los planetas se mantienen cerca del sol por la gravedad, mientras que los electrones se mantienen cerca del núcleo por algo llamado una fuerza de Coulomb)
