
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:35.
- Última modificación 2025-01-22 16:57.
Así que nosotros calcular es tomando el peso masa de cada uno de los isótopos y sumarlos. Entonces, por primera vez masa , multiplicaremos 0.50% de 84 (amu - masa atomica unidades) = 0,042 amu, y sumarlo al 9,9% de 86 amu = 8,51 amu, y así sucesivamente.
Posteriormente, uno también puede preguntarse, ¿cómo se calcula la masa atómica promedio?
Calcular la masa atómica promedio los masa atómica promedio de un elemento es la suma de la masas de sus isótopos, cada uno multiplicado por su abundancia natural (el decimal asociado con el porcentaje de átomos de ese elemento que son de un isótopo dado). Masa atómica promedio = f1METRO1 + f2METRO2 +…
También sepa, ¿qué tres tipos de información se necesitan para calcular una masa atómica promedio? El número de isótopos que existen para el elemento. los Atómico Número para el elemento. El porcentaje de abundancia de cada isótopo.
También se puede preguntar, ¿cuál es el valor más cercano a la masa atómica del estroncio?
Estroncio . En su informe de 1961, la Comisión recomendó Ar(Sr) = 87,62 basado en el masa -determinación espectrométrica de Nier. Esta valor fue revisado a Ar(Sr) = 87.62 (1) en 1969 y permanece sin cambios desde entonces.
¿Qué tiene una masa de 1 amu?
Una unidad de masa atómica (simbolizada AMU o amu) se define exactamente como 1/12 de la masa de un átomo de carbono-12. El átomo de carbono-12 (C-12) tiene seis protones y seis neutrones en su núcleo. En términos imprecisos, una UMA es el promedio de la protón masa de descanso y el neutrón masa de descanso.
Recomendado:
¿Cuál es la masa atómica promedio de un átomo?

La masa atómica promedio de un elemento es la suma de las masas de sus isótopos, cada una multiplicada por su abundancia natural (el decimal asociado con el porcentaje de átomos de ese elemento que son de un isótopo dado). Masa atómica promedio = f1M1 + f2M2 +
¿Cuál es el color de la llama del estroncio?

Pruebas de llama Color del elemento Rojo rubidio (rojo violeta) Azul cesio / violeta (ver más abajo) Rojo anaranjado cálcico Rojo estroncio
¿Cómo se determina la masa atómica promedio que se muestra en la tabla periódica?

La masa atómica promedio de un elemento se calcula sumando las masas de los isótopos del elemento, cada una multiplicada por su abundancia natural en la Tierra. Al hacer cualquier cálculo de masa que involucre elementos o compuestos, siempre use la masa atómica promedio, que se puede encontrar en la tabla periódica
¿Cómo se calcula la masa atómica del boro?
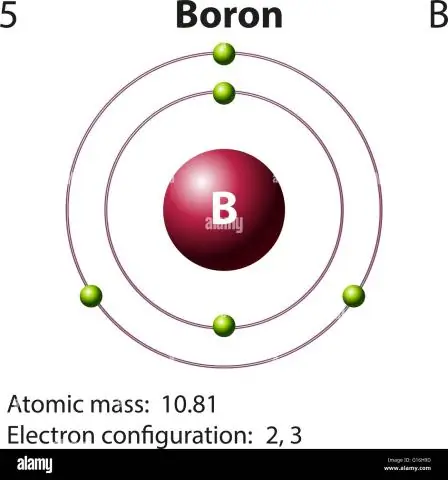
Para el boro, esta ecuación se verá así: 5 protones + 5 neutrones = 10 unidades de masa atómica (UMA) o, para el isótopo de boro más común (aproximadamente 5 protones + 6 neutrones = 11 UMA)
¿Cómo se calcula el promedio en PHP?
Siempre que desee obtener el promedio, divida la suma por el recuento (cuidando el caso del recuento == 0, por supuesto). Siempre que desee incluir un nuevo número, agregue el nuevo número a la suma e incremente el recuento en 1
