
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-11-26 05:36.
- Última modificación 2025-01-22 16:57.
Puede ver más detalles sobre cada unidad de medida: peso molecular de California ( OH ) 2 o gramos Este compuesto también se conoce como Calcio Hidróxido. La unidad base del SI para la cantidad de sustancia es la Topo . 1 Topo es igual a 1 moles Ca ( OH ) 2 o 74,09268 gramos.
Además de esto, ¿cuál es la masa de un mol de Ca Oh 2?
Respuesta y explicación: el molar masa de calcio hidróxido, es decir California ( OH ) 2 es 74 gramos por Topo (g / mol).
Además, ¿cuál es la masa de 1,5 moles de co2? Respuesta: Hay 66 g CO2 en 1,5 mol de CO2.
Considerando esto, ¿cuál es la masa de 0.50 mol de Ca Oh 2?
los masa molar de calcio hidróxido, California ( OH ) 2 , es de 74,092 g / mol.
¿Cuántos moles hay en 4.5 kg de Ca Oh 2?
61 lunares
Recomendado:
¿Cuál es la razón de moles de agua a moles de CuSO4?

Divida el número de moles de agua perdidos por el número de moles de sal anhidra para obtener la relación entre moléculas de agua y unidades de fórmula. En nuestro ejemplo, 0,5 moles de agua ÷ 0,1 moles de sulfato de cobre = proporción 5: 1. Esto significa que por cada unidad de CuSO4 presente, tenemos 5 moléculas de agua
¿Cuál es la masa de 0.921 moles de gas dióxido de azufre?

La unidad base del SI para la cantidad de sustancia es el mol. 1 mol es igual a 1 mol de dióxido de azufre, o 64,0638 gramos
¿Cuál es la diferencia entre la masa de un protón y la masa de un electrón?
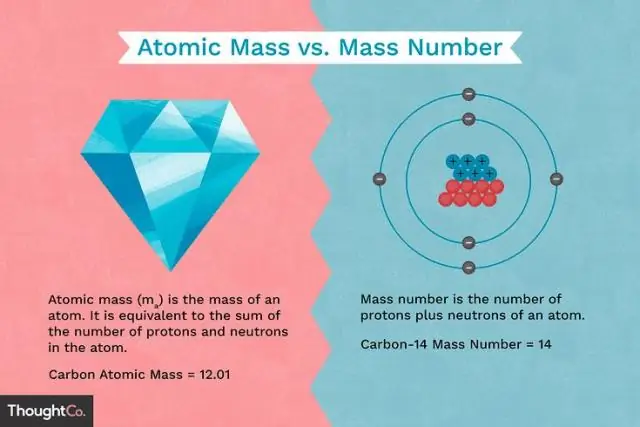
Los protones y los neutrones tienen aproximadamente la misma masa, pero ambos son mucho más masivos que los electrones (aproximadamente 2000 veces más masivos que un electrón). La carga positiva de un protón es igual en magnitud a la carga negativa de un electrón
¿Cuál es la masa de 3,5 moles de cobre?

La masa de Cu en gramos se puede obtener multiplicando la masa en amu por el número de Avogadro. Por lo tanto, la masa de 3,5 moles de Cu es 3,69 x 10 & menos 22 gramos 3,69 x 10 &menos; 22 gramos
¿Cómo se resuelven los problemas de masa de masa de reactivo limitante?

Encuentre el reactivo limitante calculando y comparando la cantidad de producto que producirá cada reactivo. Equilibre la ecuación química de la reacción química. Convierte la información dada en lunares. Use la estequiometría para cada reactivo individual para encontrar la masa del producto producido
