
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:35.
- Última modificación 2025-01-22 16:57.
los espectro de emisión del sol . los sol emite electromagnético radiación en una amplia gama de longitudes de onda. El máximo en el espectro de emisión solar está a unos 500 nm, en la parte azul verdosa del visible espectro . Además de la luz visible, la sol emite ultravioleta radiación e infrarrojos radiación.
Asimismo, ¿qué tipo de espectro emite el sol?
los El sol emite radiación a través de la electromagnética espectro , desde rayos X de energía extremadamente alta hasta ondas de radio de longitud de onda ultralarga, y todo lo que se encuentre en el medio. El pico de esta emisión ocurre en la porción visible del espectro.
Además de lo anterior, ¿qué revelan estos espectros sobre los tipos de elementos del sol? los espectros de El sol y las estrellas exhibían líneas brillantes y oscuras llamadas líneas de Fraunhofer. Se demostró que estos eran causados por elementos emitiendo o absorbiendo luz en longitudes de onda específicas. Porque cada elemento emite o absorbe luz solo en longitudes de onda específicas, se puede determinar la composición química de las estrellas.
Aquí, ¿el sol tiene un espectro de emisión o absorción?
Estrellas emisión proviene de la radiación térmica, que será aproximadamente igual a la radiación del cuerpo negro. Sin embargo, parte de esto espectro estarán absorbido por las capas externas de esta estrella. Es cierto que absorción líneas y emisión las mentiras coinciden, por lo que estas frecuencias se emitido.
¿Qué tipo de líneas espectrales son visibles en el espectro del sol?
Hay dos tipos de líneas espectrales en el visible parte de la electromagnética espectro : Emisión líneas - aparecen como colores discretos líneas , a menudo sobre un fondo negro, y corresponden a longitudes de onda de luz específicas emitidas por un objeto.
Recomendado:
¿Qué causa las líneas en el espectro de emisión de los elementos?

Las líneas de emisión ocurren cuando los electrones de un átomo, elemento o molécula excitado se mueven entre niveles de energía y regresan al estado fundamental. Las líneas espectrales de un elemento o molécula específicos en reposo en un laboratorio siempre ocurren en las mismas longitudes de onda
¿Qué causa el espectro de emisión de un elemento?

Los espectros de emisión atómica surgen de electrones que caen de niveles de energía más altos a niveles de energía más bajos dentro del átomo, se liberan fotones (paquetes de luz) con longitudes de onda específicas
¿En qué se diferencia un espectro de emisión atómica de un espectro continuo?

Espectro continuo: un espectro que tiene todas las longitudes de onda sin espacios en un amplio rango. Espectro de emisión: cuando un electrón en estado excitado se mueve a un nivel de energía más bajo, emite una cierta cantidad de energía en forma de fotones. El espectro para esta transición consta de líneas porque los niveles de energía están cuantificados
¿Es el espectro de emisión atómica una gama continua de colores?

T / F Al igual que el espectro visible, un espectro de emisión atómica es una gama continua de colores. V / F Cada elemento tiene un espectro de emisión atómica único. V / F El hecho de que solo ciertos colores aparezcan en el espectro de emisión atómica de un elemento indica que solo se emiten ciertas frecuencias de luz
¿Por qué el espectro de absorción de la clorofila ay el espectro de acción de la fotosíntesis es diferente?
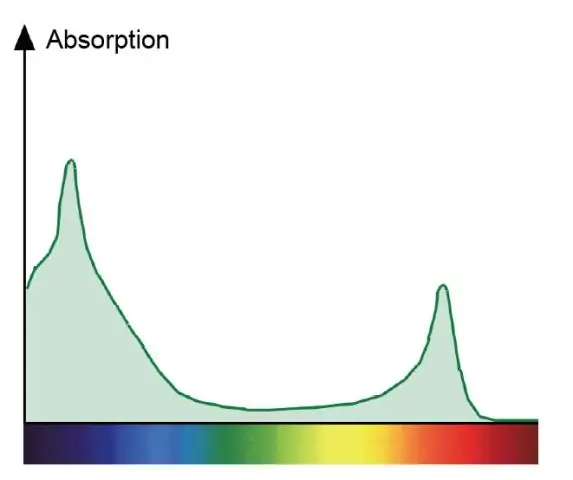
Un espectro de absorción muestra todos los colores de la luz absorbidos por una planta. Un espectro de acción muestra todos los colores de luz que se utilizan en la fotosíntesis. Las clorofilas son los pigmentos verdes que absorben el rojo y el azul y participan directamente en la fotosíntesis
